Врожденный дефект межжелудочковой перегородки (ВДМЖП; Ventricular septal defect) — это патология сердца, при которой возникают нарушения в формировании перегородки между левым и правым желудочками еще во время развития плода в утробе. В результате сердечные камеры начинают взаимодействовать между собой, что может привести к развитию сердечной недостаточности .
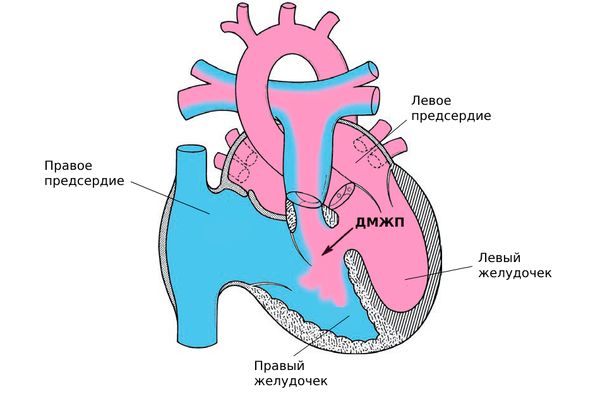
Врожденный дефект межжелудочковой перегородки [23]
Формирование сердца с крупными сосудами происходит с 3-й по 8-ю неделю беременности, а непосредственно разделение желудочков перегородкой — примерно с 32–33-го по 62–63-й дни . Отсчет ведется со дня оплодотворения яйцеклетки.
ВДМЖП может являться самостоятельным пороком сердца или входить в состав более сложных аномалий, например, тетрады Фалло или двойного отхождения крупных сосудов от правого желудочка. При тетраде Фалло дети без ВДМЖП могут выжить, в то время как при двойном отхождении дефект служит единственным путем оттока крови из левого желудочка и является жизненно важным для выживания ребенка.
Частота встречаемости ВДМЖП
За исключением стеноза аортального клапана, ВДМЖП считается наиболее распространенным врожденным пороком сердца (20–30 % от общего числа). У мальчиков и девочек он встречается примерно с одинаковой частотой .
Поскольку ВДМЖП является врожденным пороком сердца, чаще всего он выявляется в детском возрасте. В общем, ВДМЖП, как правило, диагностируют в младенчестве, и чем старше ребенок, тем меньше вероятность обнаружить этот дефект, поскольку некоторые небольшие аномалии могут закрыться самостоятельно .
Причины ВДМЖП
Существует множество факторов риска, но наиболее часто ВДМЖП встречается у детей, чьи кровные родственники также имеют врожденные пороки сердца . Установлено, что в семьях, где у близких родственников выявлен ВДМЖП (включая любые сложные врожденные аномалии сердца, в которые входит ВДМЖП), риск развития порока у ребенка немного выше, чем в здоровой популяции . При этом наличие изолированного дефекта межпредсердной перегородки или открытого артериального протока не увеличивает риск развития ВДМЖП у родственников.
К формированию любого врожденного порока сердца, включая ВДМЖП, могут привести такие факторы как:
- вредные привычки матери, вроде курения, употребления алкоголя и наркотиков во время беременности;
- инфекционные заболевания матери во время беременности, особенно вирусные (краснуха, ветряная оспа и другие);
- воздействие вредных факторов окружающей среды в первом триместре.
При обнаружении одинаковых признаков следует проконсультироваться с врачом. Не рекомендуется заниматься самолечением, так как это опасно для вашего здоровья!
Симптомы дефекта межжелудочковой перегородки
Диагностика ДМЖП зависит главным образом от размеров самого дефекта: чем он больше, тем более ярко проявляются симптомы.
Обычно при очень больших дефектах, когда давление в желудочках одинаковое, шум при аускультации практически не слышен. Однако родители могут заметить, что ребенок стал реже есть, так как ему тяжело дышать во время кормления, он перестает сосать для того, чтобы отдышаться, или делает это медленнее, также ребенок может сильно потеть во время еды. Все эти симптомы являются признаками развивающейся сердечной недостаточности, то есть осложнений, а не самого ДМЖП: основным симптомом дефекта является отсутствие или изменение шума, а остальные признаки уже вызваны сердечной недостаточностью. При появлении подобных симптомов необходимо немедленно обратиться к педиатру и выполнить эхокардиографию.
Маленькие дефекты имеют менее яркую клиническую картину — обычно едва заметную, и лишь громкий шум в сердце будет основным признаком порока. Если шум довольно грубый, его можно услышать без фонендоскопа; также иногда может быть систолическое дрожание грудной клетки в области сердца; и оба эти признака могут быть замечены родителями самостоятельно. В любом случае, при появлении каких-либо подозрений на наличие врожденного порока сердца необходимо срочно обратиться к врачу и провести эхокардиографию, чтобы выяснить, что не так с сердцем малыша.
Патогенез дефекта межжелудочковой перегородки
В здоровом сердце есть четыре камеры: правое предсердие, правый желудочек, левое предсердие и левый желудочек. В правых камерах находится кровь, бедная кислородом, которая затем поступает в лёгкие через лёгочную артерию, где обогащается кислородом. После этого она поступает в левые камеры, которые через аорту распространяют кровь, богатую питательными веществами и кислородом, по всему организму. Этот процесс повторяется с рождения и до смерти.
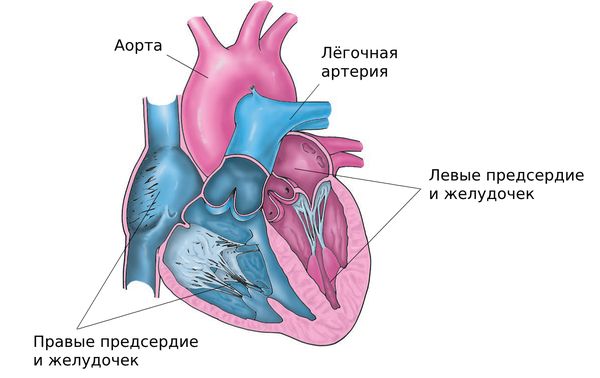
Строение сердца
У плода в утробе матери лёгкие практически не участвуют в кровообращении и не выполняют функцию газообмена. Мама обеспечивает кислородом кровь для плода. Потому что плод не дышит, лёгкие сжаты, и сосуды лёгких создают высокое сопротивление, что также повышает давление в правом желудочке. Поэтому кровь не перетекает в левый желудочек через дефект межжелудочковой перегородки.
При первом вдохе ребёнка после рождения лёгкие расширяются, сосудистое сопротивление снижается. Правому желудочку больше не нужно вырабатывать высокое давление, поэтому давление начинает снижаться. Создаётся разница в давлении между левым и правым желудочками. Часть крови, богатая кислородом, начинает утекать в правый желудочек и снова попадает в лёгкие через ДМЖП, перегружая лёгочный кровоток.
Чем больше дефект, тем сильнее перегрузка лёгких кровью. Вначале сосуды лёгких могут справиться с дополнительным объёмом крови, но со временем начнутся изменения в их стенках. Подробнее о последствиях можно узнать в разделе «Осложнения».
Классификация и стадии развития дефекта межжелудочковой перегородки
Классификация дефектов межжелудочковой перегородки зависит от их местоположения в самой перегородке. Для специалистов по детской кардиологии и кардиохирургии это важно, так как это влияет на выбор метода лечения и особенности операции.
Существует четыре основных вида дефектов:
- по типу атриовентрикулярного канала (приточные);
- мышечные (задние, средние, передние и верхушечные);
- коновентрикулярные (мембранозные дефекты, дефекты tетрада Фалло и перерыв дуги аорты с дефектом межжелудочковой перегородки);
- дефекты конусной перегородки (отточные или подлёгочные).
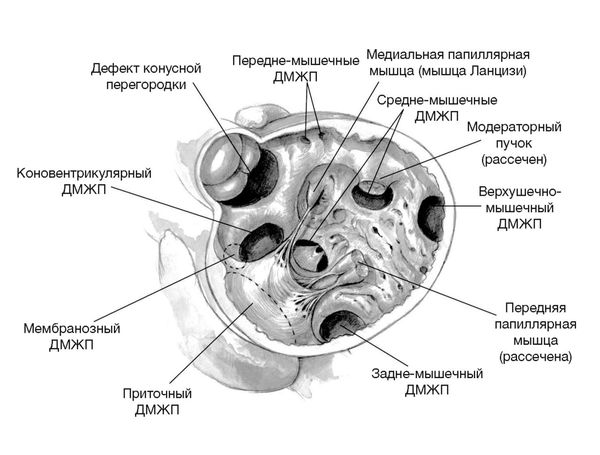
Виды дефектов межжелудочковой перегородки [21]
Наиболее распространены мембранозные дефекты коновентрикулярных, составляющие до 70–80% всех дефектов межжелудочковой перегородки. Аортальная недостаточность чаще развивается при дефекте конусной перегородки, а дефекты по типу атриовентрикулярного канала могут сочетаться со страддлингом трикуспидального или митрального клапана, что затрудняет хирургическое вмешательство. Страддлинг — это прикрепление папиллярных мышц в неправильном желудочке, что смертельно для операций.
Существует также категория дефектов, которые называются «швейцарский сыр». Это множественные дефекты, требующие особого подхода к лечению.
Гемодинамическая классификация дефектов, определяющая величину сброса крови и степень проявления симптомов, представляет большой интерес.
Согласно этой классификации, выделяют два вида дефектов:
- Маленькие дефекты — обычно не проявляют симптомов и обнаруживаются случайно;
- Большие дефекты — всегда проявляют себя через выраженные симптомы, при этом родители обращаются к врачу.
Определение дефекта как большого или маленького зависит от веса ребенка. Для младенца весом 2 кг, дефект в 4 мм может быть значимым, а для 4-килограммового младенца 6 мм дефект может быть бессимптомным.
Этапы дефекта межжелудочковой перегородки
Выделяют три этапа:
- Компенсация — организм ребенка полностью компенсирует изменения, жизнеугрожающие состояния отсутствуют.
- Субкомпенсация — начинают проявляться первые симптомы сердечной недостаточности.
- Декомпенсация — проявляются более серьезные медицинские проблемы.
Если дефекты большого размера (более 8–10 мм) не оперировать, то в результате возникнут необратимые изменения, приводящие к специфическому синдрому. Лечение в данном случае возможно только медикаментозно специфическими препаратами.
Осложнения дефекта межжелудочковой перегородки
Одним из главных осложнений является необратимая лёгочная гипертензия, другими словами — синдром Эйзенменгера. Это заболевание возникает из-за долговременной перегрузки сосудов лёгких дополнительным объёмом крови и повышенным давлением (при ДМЖП). Стенки сосудов подвергаются чрезмерному растяжению на протяжении длительного времени, что приводит к необратимым изменениям — они утрачивают свою эластичность и становятся жёсткими, как металлическая труба.
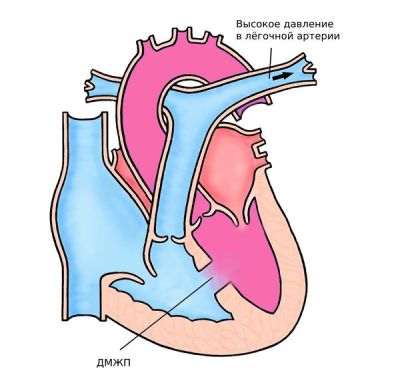
Синдром Эйзенменгера
Симптомы синдрома Эйзенменгера включают цианоз (синюшность кожи), обмороки, одышку, усталость, боль в груди, учащенное сердцебиение, а также кровохарканье, хотя оно обычно возникает позднее. Если дополнительный объем крови значителен и нет ограничений, то данный синдром может развиться уже в первом году жизни; если же есть хотя бы некоторое ограничение, то для его появления может потребоваться десятки лет. Малый дефект с высоким градиентом давления называют рестриктивным, при котором давление в желудочках равно.
К другим возможным осложнениям относятся инфекционный эндокардит левых отделов сердца и недостаточность аортального клапана, вызванная проваливанием одной из створок в дефект.
Инфекционный эндокардит может развиться у пациентов с любым видом ДМЖП независимо от размеров дефекта, пола, возраста и других факторов. При этом осложнении у 90% пациентов обычно повышается температура тела (чаще до 37,1–38,0 °C). Могут появиться общая слабость, потеря аппетита, уменьшение веса, а также характерные симптомы: узелки Ослера (болезненные подкожные узелки, обычно на подушечках пальцев), очаги Джейнуэя (безболезненные пятна на ладонях и подошвах) и пятна Рота (кровоизлияния в сетчатке глаза с белыми участками в центре). Эндокардит также может сопровождаться эмболическими осложнениями (закупорка артерий, направленных как к лёгким, так и к мозгу).
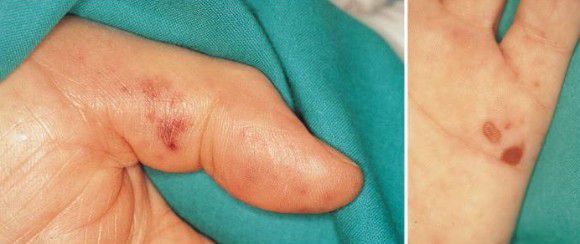
Узел Ослера (слева) и очаг Джейнуэя (справа) [22]
Недостаточность аортального клапана чаще наблюдается при коновентрикулярных дефектах и дефектах конусной перегородки. Основным симптомом является диастолический шум в области аортального клапана, также могут появиться симптомы Мюссе (покачивание головы в такт сердечным сокращениям), «пляска каротид» (видимая пульсация общих сонных артерий) и большая разница между систолическим и диастолическим давлением.
Диагностика дефекта межжелудочковой перегородки
Поиск дефектов межжелудочковой перегородки сводится к сбору анамнеза (истории болезни), аускультации, электрокардиографии и эхокардиографии. Иногда, для количественной оценки лёгочного сосудистого сопротивления, применяется ангиография или зондирование полостей сердца.
История болезни
Во время консультации врач узнает о прохождении беременности, воздействии вредных факторов на матери (например, проживание рядом с опасными производствами, курение и употребление алкоголя в начале беременности), наличии у родителей врожденных пороков сердца.
Аускультация
При прослушивании, в зависимости от градиента давления между желудочками, слышен будет систолический шум разной интенсивности. При небольших дефектах с высоким давлением слушается сильный шум (иногда называемый «машинным») по всей области сердца. При больших дефектах, когда давление в желудочках приблизительно одинаковое, шум будет значительно тише.
Электрокардиография и эхокардиография
Изменения на электрокардиограмме могут подтолкнуть к проведению эхокардиографии. Такие изменения могут включать смещение оси сердца влево с признаками перегрузки левого крыла.
Эхокардиография — оптимальный метод для обнаружения большинства врожденных пороков сердца, включая дефекты межжелудочковой перегородки. Она точно определяет размеры, местоположение и количество дефектов, а также оценивает объем сброса крови в легочной артерии по отношению к системной циркуляции (Qp/Qs).
Чаще всего этих исследований достаточно для определения необходимости оперативного вмешательства.
Зондирование полостей сердца
Иногда зондирование полостей сердца необходимо для количественной оценки лёгочного сосудистого сопротивления и только после этого принимается решение о методе лечения.
Дифференциальная диагностика
Дифференциальная диагностика при ДМЖП чаще всего проводится внутри самого диагноза — определяется локализация, размеры и количество дефектов. Также важно различать врожденные дефекты межжелудочковой перегородки от приобретенных (в результате травмы или инфаркта миокарда с участием межжелудочковой перегородки). Следует отметить, что такие ситуации более характерны для взрослых. Например, 1–4 % пациентов развивают дефект межжелудочковой перегородки в течение недели после инфаркта.
Лечение дефекта межжелудочковой перегородки
Оперативное лечение ДМЖП — это основной способ борьбы с этим заболеванием. Поскольку большинство дефектов являются коновентрикулярными (мембранозными), операции, как правило, выполняются с обязательным вскрытием грудной клетки.
Показания к операции
Индикациями для закрытия дефектов межжелудочковой перегородки являются признаки сердечной недостаточности и перегрузки левых отделов сердца у детей первых шести месяцев жизни.
Если сердечная недостаточность не обнаружена, врачи оценивают соотношение лёгочного и системного кровотока (Qp/Qs). Если это соотношение больше 1,5, показано проведение операции. Если показатель ниже 1,5, операция не требуется, и дефект наблюдается. Дефекты (особенно мышечные) могут закрыться или уменьшиться самостоятельно со временем. Однако возможно развитие осложнений (например, аортальной недостаточности или инфекционного эндокардита) в процессе наблюдения — это также станет показанием для хирургического вмешательства. Перед операцией при эндокардите может потребоваться антибиотикотерапия или лечение противогрибковыми средствами для устранения воспаления. В случае отсутствия показаний к операции по поводу инфекционного эндокардита (левосторонние вегетации более 10 мм или критические проблемы с клапанами), в первую очередь проводится антибиотикотерапия — эмпирическая, т. е. прием антибиотиков широкого спектра до получения результатов анализов, или с учетом результатов посевов.
Перед операцией младенцы должны проходить обследование ежемесячно до года, если показания к хирургическому лечению не появятся раньше; после года частота обследований уменьшается постепенно до одного раза в год.
Хирургическое вмешательство с открытым доступом
Операции обычно проводятся с доступом через грудину. Во время основной части операции функции сердца и легких выполняется специальным аппаратом искусственного кровообращения. Дефекты закрываются заплатой, чаще всего из бычьего перикарда, но могут использоваться и синтетические материалы. После хирургического лечения восстановление состояния пациента очень зависит от его состояния в момент операции. В среднем реабилитация в стационаре занимает до 10–14 дней. После операции контрольные осмотры проводятся через месяц, затем через 3, 6, 12 месяцев и затем каждый год, если нет никаких жалоб.
Эндоваскулярные процедуры
Эндоваскулярное закрытие дефекта осуществляется специальным устройством, которое доставляется по проводнику через бедренную вену, и не требует вскрытия грудной клетки. Однако у этого метода есть ограничения: местоположение дефекта и вес пациента. Обычно такие операции выполняются только при мышечных дефектах в средней части перегородки; в редких случаях они могут проводиться и при мембранозных дефектах, но это практикуется единично. Еще одним ограничением является вес ребенка, так как для введения катетера в бедренную вену используются крупные устройства. По данным фирмы Abbot (производителя устройств Amplatzer), у детей с весом менее 5,2 кг наблюдались неприятные последствия, поэтому таким детям не рекомендуется эндоваскулярная операция. Также отмечается, что эта процедура нежелательна у пациентов, у которых расстояние от края дефекта до клапанов менее 4 мм .
На практике эндоваскулярное закрытие не так часто применяется, так как большинство дефектов мембранозные (с краями на кольце аортального и трикуспидального клапанов). На оставшиеся, подходящие для закрытия эндоваскулярным методом дефекты, приходится не так много операций.
Операции при дефектах по типу «швейцарского сыра»
Закрытие всех дефектов у ребенка первого года жизни сразу, особенно при дефектах по типу «швейцарского сыра», довольно сложная задача. Операции при таких дефектах требуют много времени и могут нанести сердцу значительный ущерб, поэтому показатели выживаемости у детей такого возраста после первично-радикальной коррекции ДМЖП по типу «швейцарского сыра» невысоки. С возрастом и набором веса у детей становится легче проводить операции внутри сердца (находить все дефекты и закрывать их качественно) и реабилитация после операции также становится проще.
Существует двухэтапный метод коррекции, при котором сначала проводится операция по сужению легочной артерии. Для этого используется специальная синтетическая полоска — манжет. Цель такой операции заключается в уменьшении перегрузки сосудов легких из-за дополнительного объема крови и предотвращении развития сердечной недостаточности. Когда ребенок вырастет и наберет вес, манжету удаляют и одновременно закрывают несколько дефектов.
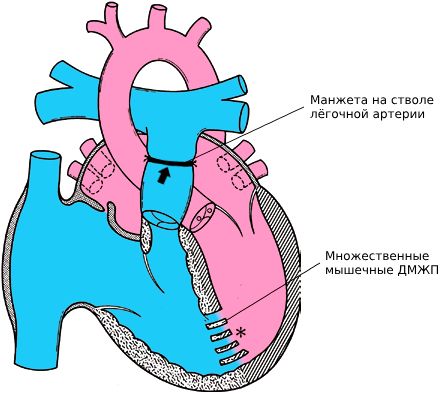
Сердце с множественными мышечными ДМЖП после суживания лёгочной артерии
Возможные осложнения после операции
Осложнения, связанные с самим хирургическим вмешательством, могут встречаться довольно часто. После операции может возникнуть временная или устойчивая атриовентрикулярная блокада, требующая установки электрокардиостимулятора. Также существует риск развития дисфункции клапанов (в основном аортального или трихосторчатого) в результате наложения заплаты или установки окклюдера .
При наличии возможности пластической операции при развитии дисфункции клапанов в детском возрасте этот метод всегда предпочтителен; если это невозможно, может проводиться протезирование клапанов — механические/биологические протезы, аутографты (операция Росса).
Прогноз. Профилактика
Некоторые небольшие дефекты межжелудочковой перегородки в 20–30 % случаев имеют тенденцию закрываться самостоятельно. Бывают случаи, когда даже относительно крупные дефекты могут уменьшиться или закрыться спонтанно. В случае если дефект не закрывается и не вызывает серьезных нарушений в работе сердца, рекомендуется проводить периодическое наблюдение (раз в год для детей старше года без жалоб).
Летальность во время или после операции не превышает 1 %. После хирургического лечения качество жизни пациентов и их продолжительность такие же, как у здоровых людей.
Специфических методов профилактики врожденных пороков сердца не существует. Рекомендации о здоровом образе жизни матери, отказ от пагубных привычек, избегание опасных средовых условий и заразных болезней имеют лишь неспецифический характер и даже их соблюдение не дает 100% гарантии на положительный результат.
Список литературы
- Ассоциация сердечно-сосудистых хирургов России. Дефект межжелудочковой перегородки: клинические рекомендации МЗ РФ. — М., 2021. — 58 с.
- Hoffman J. I., Kaplan S. The incidence of congenital heart disease // J Am Coll Cardiol. — 2002. — № 12. — Р. 1890–1900. ссылка
- Schoenwolf G. C., Bleyl S. B., Brauer P. R., Francis-West P. H. Larsen’s human embryology. — 5th edition. — Elsevier Health Sciences, 2015. — P. 288–290.
- Шарыкин А. С. Врождённые пороки сердца: руководство для педиатров, кардиологов, неонатологов. — 2-е издание. — М.: Теремок, 2009. — 384 с.
- Бокерия Л. А., Гудкова Р. Г. Сердечно-сосудистая хирургия — 2021. Болезни и врожденные аномалии системы кровообращения. — М., 2022. — С. 133–189.
- Wernovsky G., Anderson R. H., Krishna К. et al. Anderson’s Pediatric Cardiology. — 4-th edition. — Elsevier E-Book, 2020. — 2526 p.
- Гриппи М. А. Патофизиология лёгких. — 2-е издание, исправленное. — М.: Бином, 2022. — 304 с.
- Morton S. U., Brodsky D. Fetal Physiology and the Transition to Extrauterine Life // Clin Perinatol. — 2016. — № 3. — Р. 395–407. ссылка
- Praagh R. V. Congenital Heart Disease: A Clinical, Pathological, Embryological, And Segmental Analysis. — Elsevier, OHCE, 2022. — Р. 767–817.
- Кривощеков Е. В., Ковалева И. А., Шипулина В. М. Врождённые пороки сердца: справочник для врачей. — Томск: STT, 2009. — 286 с.
- Kidd L., Driscoll D. J., Gersony W. M. et al. Second natural history study of congenital heart defects. Results of treatment of patients with ventricular septal defects // Circulation. — 1993. — Vol. 87. — P. I38–51. ссылка
- Jonas R. A. Comprehensive Surgical Management of Congenital Heart Disease, Second Edition. — CRC Press, 2014. — P. 331–346.
- Bronzetti G. Atlas of Pediatric and Youth ECG. — Springer International Publishing, 2018. — 320 p.
- Lai W. W., Mertens L. L., Cohen M. S., Geva T. Echocardiography in Pediatric and Congenital Heart Disease, From Fetus to Adult. — 2nd edition. — Jonh Wiley & Sons Ltd, 2016. — P. 215–230.
- Kirklin j. K., Blackstone E. H. Kirklin/Barratt-Boyes Cardiac Surgery. — 4th edition. — Elsevier Saunders, 2013. — P. 446–459, 1275–1319.
- Artemiou P., Gasparovic I., Hudec V., Hulman M. Optimal therapeutic strategy for postinfarction ventricular septal defect // J Card Surg. — 2022. — № 8. — Р. 2511. ссылка
- Хапаев С. А. Хирургическое лечение осложнений инфаркта миокарда левого желудочка и межжелудочковой перегородки: автореф. дис. … д-ра мед. наук: 14.00.44, 14.00.06. — Новосибирск, 2005. — 40 с.
- Beerman L. B. Eisenmenger Syndrome // MSD Manual. — 2023.
- Shaddy R. E., Penny D. J., Feltes T. F. et al. Moss & Adams’ Heart Disease in Infants, Children and Adolescents Including the Fetus and Young Adult, Volume I–II. — 10th edition. — Wolters Kluwer, 2022. — P. 2313–2317.
- Hoffman J. I. E. Congenital Heart Disease: Incidence and Inheritance. Congenital Heart Disease: Incidence and Inheritance // Pediatric Clinics of North America. — 1990. — № 1. — Р. 25–43.ссылка
- Jonas R. A. Comprehensive Surgical Management of Congenital Heart Disease. — 2nd edition. — CRC Press, 2014. — 333 р.
- Armstrong G. P. Infective Endocarditis // MSD Manual. — 2022.
- Park I. S. An Illustrated Guide to Congenital Heart Disease. — Springer Nature Singapore Pte Ltd., 2019. — P. 34, 50.
- Structural Interventions: Congenital Heart Defects // Abbott. [Электронный ресурс]. Дата обращения: 13.10.2023.
Факторы риска и предрасполагающие условия для ВДМЖП
Среди основных факторов риска для ВДМЖП можно выделить наследственную предрасположенность, формирование пороков сердца у матери и даже воздействие некоторых инфекций на процесс развития эмбриона. Недостаточности питания и различные токсические вещества также могут оказать негативное влияние на формирование сердечной патологии у ребенка.
Важно помнить, что правого и левого дефектов межжелудочковой перегородки имеют различные факторы риска, и поэтому методы профилактики и лечения должны быть индивидуализированы под каждый конкретный случай. Поэтому к обязательным мерам следует отнести своевременное обследование женщин до и во время беременности, чтобы выявить возможные риски и предпринять необходимые меры для предотвращения возникновения дефекта межжелудочковой перегородки.
Современные методы лечения дефекта межжелудочковой перегородки
Одним из современных методов лечения дефекта межжелудочковой перегородки является оперативное вмешательство. В зависимости от размера и местоположения дефекта, хирурги могут применять различные техники, включая использование тканей ребра или искусственных материалов для закрытия дефекта.
Другим эффективным методом является катетеризация, при которой через сосуды пациента вводятся специальные устройства для закрытия дефекта без необходимости хирургического вмешательства. Этот метод является менее инвазивным и способствует быстрому восстановлению пациента.
Последствия неоперированного ВДМЖП во взрослом возрасте
Неоперированный дефект межжелудочковой перегородки может привести к сложным последствиям во взрослом возрасте. Во-первых, из-за близкой структуре отхождения правого и левого клапана аортального протока, где часто встречаются изолированные ВДМЖП, возрастает вероятность формирования сложных заболеваний сердца.
| Причины | Дни младенчества | Процент |
|---|---|---|
| краснуха | 3-й | 20–30% |
| изоляция | 8-ю | 62–63-й |
| пороки | вообще | к 100% |
У девочек вероятность формирования сложных заболеваний структуры сердца, связанных с ВДМЖП, начинаются с раннего возраста, где отсчёт идет в днях. В 3-й день после рождения у ребёнка может быть выявлен закрывающийся дефект межжелудочковой перегородки. Во всех случаях, где не оперировали ВДМЖП в младенчестве, необходимо пристальное внимание к состоянию сердца взрослого пациента, так как последствия могут быть серьезными.
Современные тенденции в диагностике и лечении дефекта межжелудочковой перегородки
- Диагностика в настоящее время ведется с помощью современных методов, таких как ультразвуковое исследование, компьютерная томография и магнитно-резонансная томография.
- Лечение ДМЖП может проводиться как консервативно, так и хирургически, в зависимости от тяжести и формы дефекта.
- Существуют специализированные центры, в которых проводится оперативное лечение с применением современных технологий.
Помимо этого, проводятся исследования, направленные на выявление факторов риска и профилактику развития ДМЖП. Так, например, родители, у которых уже есть ребенок с таким дефектом, должны обратить особое внимание на планирование беременности и профилактику заболеваний, которые могут возникнуть во время беременности.
Видео по теме:
Вопрос-ответ:
Какие последствия может иметь дефект межжелудочковой перегородки для организма?
Дефект межжелудочковой перегородки может привести к развитию сердечной недостаточности, так как кровь из правого желудочка перетекает в левый, обогащаясь при этом кислородом меньше, чем обычно. Это может вызвать утомляемость, одышку, сердцебиение и другие симптомы сердечной недостаточности.
Каков период формирования перегородки между желудочками сердца?
Формирование перегородки между желудочками сердца происходит примерно с 32–33-го по 62–63-й дни развития плода, которые приходятся на 5-9 недели беременности. В это время происходит разделение желудочков и формирование перегородки, разделяющей правый и левый желудочки.
Как возникает дефект межжелудочковой перегородки?
Дефект межжелудочковой перегородки возникает в результате нарушения развития сердца внутриутробно. Обычно это происходит из-за генетических факторов или воздействия внешних негативных факторов на развивающийся плод во время беременности.
Какие типы дефектов межжелудочковой перегородки могут встречаться?
Дефект межжелудочковой перегородки может встречаться изолированно или в сочетании с другими пороками сердца. В зависимости от размера и местоположения дефекта различают неклозурные, малые, средние и большие ДМЖП.